
法规背景: 瑞士作为欧洲的国家,既不是EU的成员也不是EEA的成员。 瑞士与欧盟的双边协议在2021年5月26日未达成一致而终止。因此从2021年5月26日开始,瑞士的医疗器械管理依据是由其主管当局Swiss Medic在2020年7月1日发布的新版MedDO法规。 新旧版本MedDO法规与MDR/IVDR的关系目前...

法规现状英国脱欧后,UKCA 标志于 2021 年 1 月在英国大不列颠 (Great Britain) 正式生效。一些分类的医疗器械可能需要持有 UKCA 认证。UKCA的过渡期将持续至 2023 年 6 月 30 日,以便进行从现有 CE 证书向 UKCA 证书的变更。然而,英国新立法的咨询已经结束,因此新的英国立...

所有在沙特上市的医疗器械均应获得沙特MDMA证书。沙特MDMA证书,全称Medical Device Marketing Authorization, 是目前医疗器械在沙特上市的唯一合规路径。无论何种风险等级的医疗器械在上市前必须获得MDMA证书。 境外医疗器械制造商若要申请MDMA证书,必须委派一名当地个人或实...

欧盟国家对于眼镜、眼镜镜片出口按医疗器械管控,像轮椅,拐杖,护具,洗澡椅,座便器,助行器,矫正器,非灭菌无纺布制品,光学眼镜等按欧盟医疗器械新法规MDR分类,MDR CE都是属于欧盟普通一类Class I的产品。MDR法规对于普通Class I类没有提出认证要求,MDR法规下,普通I类也不需要公告机构评审,MDR法规下...

ISO13485认证需要什么材料ISO13485:2016标准的全称是《医疗器械 质量管理体系 用于法规的要求》,对医疗器械生产企业的质量管理体系提出了专用要求,为医疗器械的质量达到安全有效起到了很好的促进作用。 适用范围本标准适用于进行医疗器械的设计和开发、生产、安装和服务或相关服务的设计、开发和提供等相关行业。在标...
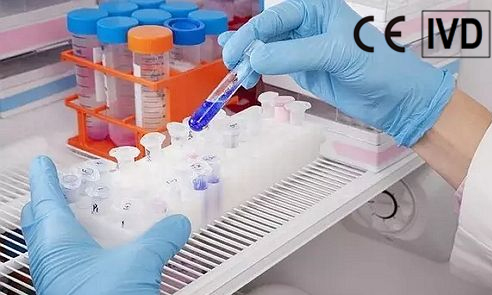
检测试剂盒如何选择适合的欧代?合格的欧盟授权代表EU-REP应当:1) 具有专业的法规和法律能力,帮助企业咨询、了解并响应欧盟法规。选择专业的欧盟授权代理机构,需要充分考察欧代的沟通能力、响应时效、信息准确性、规模和品牌、行业口碑等,是选择合格Authorized Representative的重要依据。2) 合法高效...

电动轮椅CE认证是电动轮椅进入欧盟市场销售所需的产品认证,主要从产品安全角度考虑。目前,我国电动轮椅行业的生产主要集中在上海、佛山、永康、天津和丹阳等地。电动轮椅、拐杖、手杖、助行器、坐便椅、护理床、气垫床等康复器材用品在海外市场具有广阔的前景。以下是电动轮椅出口欧盟办理CE认证的相关检测要求。 在将轮椅推向欧盟市...

担架、急救包、颈托、移位车、止血带、冰袋、棉球、弹性绷带、医用胶带、创可贴、自粘绷带、乳胶手套、丁腈手套、急救毯、三角绷带、医用剪、听诊器、轮椅等产品欧盟MDR法规分类为CLASS I,对于 I类的产品,欧盟强制要求2021 年 5月 25 号强制实施MDR2017/745新法规;老MDD法规不管我们的CE证书是否在有...

欧盟医疗器械MDR法规强制实施时间:2021年5月26号 法规规定:从2021年5月26号开始公告机构不能按照MDD颁发CE证书,目前I*及以上风险等级产品认证机构已不再受理MDD指令的认证申请。MDD失效时间:2024年5月27号 2024年5月27号起,企业持有的MDD指令的CE证书全部失效。 请注意以下新更新通知...

欧盟医疗器械MDR法规强制实施时间:2021年5月26号 法规规定:从2021年5月26号开始公告机构不能按照MDD颁发CE证书,目前I*及以上风险等级产品认证机构已不再受理MDD指令的认证申请。MDD失效时间:2024年5月27号 2024年5月27号起,企业持有的MDD指令的CE证书全部失效。 请注意以下新更新通知...

新冠抗原检测试剂出口欧盟国家CE认证、商务部白名单申请流程: 现阶段,新型冠状病毒检测试剂进入欧盟市场,制造商既可以选择遵照IVDD(98/79/EC)指令的要求,也可以选择遵照IVDR(Regulation (EU) 2017/746)法规的要求,通过CE认证后合法上市。新冠病毒检测试剂的主要分类按照IVDD指令中的...

2024年,康复医疗器械领域的出口额达到了百亿元级别,同比增长12.39%,且连续5年稳步增长。首先需要明确的是,电动轮椅、电动代步车、拐杖、助行器、沐浴椅、病床等产品在新欧盟医疗器械法规(MDR)下属于CE I类,即低风险产品,管控相对较松。 电动轮椅、电动代步车、拐杖、助行器、沐浴椅、手动病床制造商需要选择欧盟授权...

随着欧盟IVDR 法规延期 ,IVD企业获得更长缓冲期,尤其是利好了国内新冠试剂厂家。 在IVDR延期的过渡期直至2025年5月26日,新冠试剂厂家可以按IVDDother 类办理欧盟注册,欧代,CE技术文件,DOC完成CE合规出口欧盟。 新冠检测试剂盒CE认证要求和流程: 新冠检测试剂盒可以分为自测版和专用版,合规路...

像常见康复器械,如电动轮椅,手动轮椅,助行器,洗澡椅,坐便器,牵引器,电动病床,手动病床,医用夹板,肩部护肘、无纺布制品口罩隔离衣防护服;牙科耗材、卫生用品护垫纸尿裤等产品都是属于欧盟一类产品,出口到欧盟地区都需要按医疗器械管控,加贴CE标识。 我司能够提供CE认证、欧盟授权代表、欧盟注册;UKCA认证、英代、MHRA...

在这个充满机遇与挑战的时代,中国医疗器械制造商正以前所未有的速度走向世界,而沙特市场无疑是其中的一块重要拼图。 自去年开展业务至今,FDASUNGO机构已成功助力超过110家中国制造商在沙特市场取得重大突破,为他们赢得了宝贵的沙特医疗器械与体外诊断器械MDMA注册证书。 这一成绩不仅彰显了中国医疗器械行业的...