
电动轮椅CE认证是电动轮椅进入欧盟市场销售所需要做的产品认证,主要是从产品安全方面进行考虑。目前,我国电动轮椅行业发展生产主要集中于上海、佛山、天津和永康、丹阳等地。轮椅,拐杖,手杖,助行器,坐便椅,护理床,气垫床,成人纸尿裤,护理垫,翻身垫,脚圈,坐垫圈,等康复器材用品,康复设备海外市场市场前景广大。我们重点来了解下...

全球医疗护理用品贸易中,成人纸尿裤类产品的跨国流通需满足目标市场法规要求。本文梳理主要出口地区的认证规范与实施要点,助力企业高效完成合规布局。 【欧盟市场准入:MDR CE认证】 法规框架:医疗器械法规(MDR 2017/745) 分类管理:I类非灭菌产品适用自我声明路径 核心步骤: 编制CE技术文档(含生物相容性...

喜讯!广州某科技无线超声探头项目成功斩获MDR CE认证,开启全球市场新征程! 新春捷报,再创佳绩! 广州某科技有限公司自主研发的无线超声探头项目,近日成功通过欧盟医疗器械新法规MDR CE认证,并荣获由国际权威认证机构天祥(Intertek)颁发的CE证书!这标志着该产品在安全性、有效性和质量方面均已达到国际...

近日,由我们提供专业咨询支持的湖北某敷料企业,其生产的水体胶敷料和硅酮胶泡沫敷料成功通过欧盟医疗器械法规(MDR)认证审核。经过双方近半年的密切配合,顺利取得了认证证书! 此次MDR认证的通过,不仅高度认可了该企业产品的品质,也充分肯定了我们咨询团队的实力。众所周知,MDR认证在行业内以严格著称,顺利通过认证,展示了...

首先电动轮椅,手动轮椅,助行器,洗澡椅,坐便器,牵引器,电动病床,手动病床,医用夹板,肩部护肘等产品都是属于欧盟一类的。 MDR下的DOC和MDD的DOC不是一样的概念 从法规来说,I类普通器械也应有临床评估报告和上市后监督系统。 为什么MDR 一类的技术文件按每种产品收取? 以前MDD可以将所有产品合并一本技术文...

电动轮椅CE认证是电动轮椅进入欧盟市场销售所需的产品认证,主要从产品安全角度考虑。目前,我国电动轮椅行业的生产主要集中在上海、佛山、永康、天津和丹阳等地。电动轮椅、拐杖、手杖、助行器、坐便椅、护理床、气垫床等康复器材用品在海外市场具有广阔的前景。以下是电动轮椅出口欧盟办理CE认证的相关检测要求。 在将轮椅推向欧盟市场之...

欧盟医疗器械法规(MDR)中技术文件的主要目的是证明医疗器械满足一般安全和性能要求。无论类别如何,所有医疗设备都必须提供技术文件。MDR附件 2和附件 3涵盖了有关技术文件的要求。 MDR技术文档结构: 设备描述和规格,包括型号和配件 制造商需提供的信息 设计和制造信息 一般安全和性能要求 效益-风险分...

喜讯近日,FDASUNGO医疗助力合作伙伴IIa类产品一次性负压引流管取得TÜV莱茵签发的MDR CE证书。本次服务在展现FDASUNGO强大技术实力的同时,也帮助了企业产品实现在欧盟地区的自由流通,在走向国际市场、提升国际竞争力方面迈出了坚实的一步。FDASUNGO作为医疗器械合规领域的领先者,拥有丰富的经验和专业的...

IVDR CE认证是指符合欧洲联盟体外诊断器械法规(In Vitro Diagnostic Medical Device Regulation,IVDR)要求的体外诊断器械产品获得CE标志的认证过程。随着欧盟监管当局2021年12月21日发布公告,IVDR法规实施日期2022年5月26日起,制造商需要在此日期之后需要完...

近年来,国内电动轮椅出口欧盟的趋势呈现出稳步增长的态势。电动轮椅作为一种便捷的代步工具,在欧洲市场受到了广泛的关注和需求。欧洲国家对于辅助交通工具的需求量较大,且对产品的质量和安全性要求较高,这为国内电动轮椅出口提供了机会。同时,国内电动轮椅制造企业在技术研发和生产工艺上的不断提升,使得产品品质得到了有效提升。优质的产...

在欧洲市场上,牙科耗材的品质和安全性备受关注。为了确保质量和安全,欧盟委员会颁布了一系列严格的标准法规和指令,其中包括CE认证和ISO13485认证。 CE认证是欧洲市场通行的重要的认证标志,它是欧盟对制造业的强制认证标志。CE认证要求符合欧洲市场的技术要求和安全规定。对于牙科耗材来说,CE认证意味着该产品通过了欧...
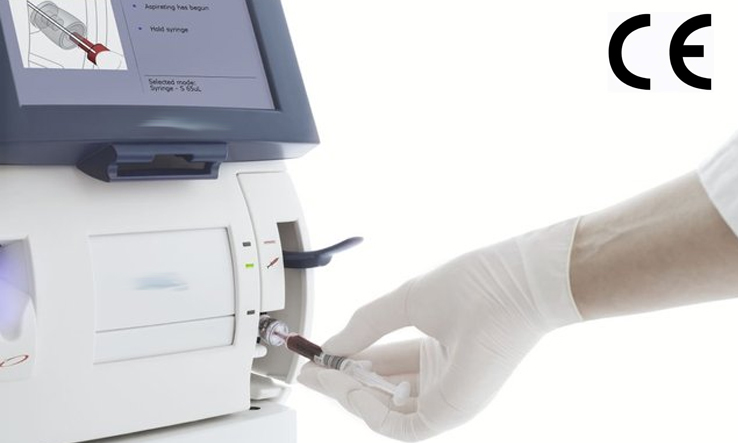
依据IVDR附录VIII分类规则Rule5,一般类的IVD仪器,例如:荧光免疫层析分析仪,酶免分析仪,PCR仪,NGS测序仪,自动核酸纯化仪,红细胞沉降率分析仪,化学发光免疫分析仪 ,全自动生化分析仪, 全自动血液细胞分析仪,尿液分析仪,血气分析仪等仪器在欧盟IVDR法规下,属于CLASS A类。 IVDR法规自202...

欧盟区是各医疗器械制造商及体外诊断(IVD)产品生产商的核心目标市场之一,而只有满足当地法规的要求,产品才能获得欧盟区市场准入资格。 医疗器械CE认证之体外诊断医疗器械IVDR分类: IVDR 2017/746号法规附录VII中详定7条规则,按医疗产品的风险程度,将产品分为Class A、Class B、Class C...
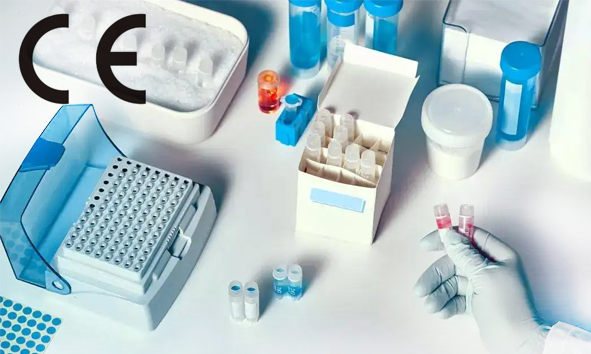
FDASUNGO荷兰公司已经为国内器械厂商成功申请IVDR CE注册证书。同时,FDASUNGO德国也已经受理部分厂商的IVDR CE注册申请。除了提供欧盟授权代表和注册服务,我们还提供IVDR技术文件编撰服务,帮助制造商全面规避合规风险。 1、哪些IVD属于Class A类呢?IVDR A类产品举例:荧光免疫分析仪...
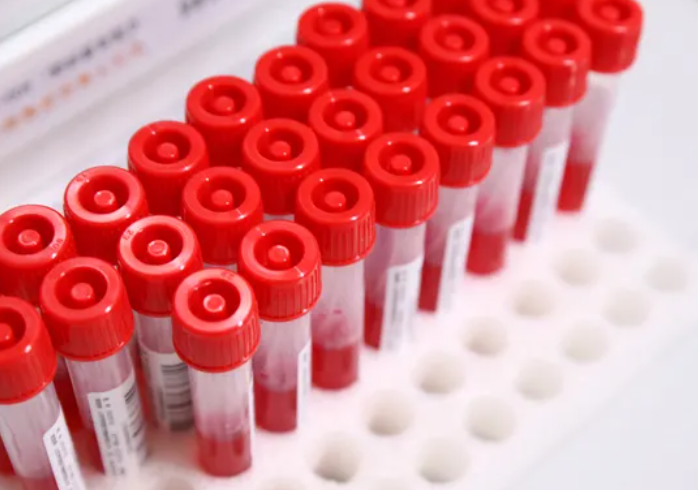
2022年,长期存在的IVDD将被IVDR取代,开启欧盟市场体外诊断器械监管新纪元。这意味着希望获得 CE 标志并在欧洲销售其产品的制造商将面临一系列新的挑战。今天我们就来看下病毒采样管、实验耗材出口欧盟IVDRCE认证怎么办理?哪些IVD属于Class A类呢?IVDR法规共有7条分类规则 IVDR分类规则5提到了...