历时4年半,英国和欧盟,于2020年的平安夜,终于达成了历史性的脱欧协议。这份《英欧贸易与合作协议》已于当地时间2020年12月31日晚11时正式生效。标志着英国正式“脱欧”,结束了其47年的欧盟成员国身份。
在脱欧之前,进入英国市场的大多数产品同其他欧盟国家一样使用CE标志(欧盟统一市场产品符合性标志)。脱欧之后,英国推出了自己的产品符合性标志UKCA以及北爱尔兰地区独有的UKNI标志。
英国的全称是大不列颠及北爱尔兰联合王国(UK),包含了大不列颠(GB)和北爱尔兰(NI)两个区域。UKCA(UK Conformity Assessed英国合格评定)标志是英国新推出的产品符合性标志,用于在英国大不列颠地区(GreatBritain,简称“GB”,包括英格兰、威尔士和苏格兰)投放到市场上的产品。

一、医疗器械UKCA合规时间限
何时会开始强制使用UKCA标志?
医疗器械的加贴UKCA标志的要求,基本可以分为UKCA合格评定和MHRA注册申报两大模块。英国MHRA在去年9月初和12月初分别发布了针对2021年医疗器械制造商如何将产品合法的投放英国市场的指南文件。这两份文件对于制造商的合规日期有明确的表述。
1)对于目前持有公告机构签发CE证书的制造商。在 2023年6月30日之前,可以继续使用CE证书将产品出口到英国(UK)市场。在2023年6月30日之后,还可以继续出口到英国的北爱尔兰(NI)市场,而不再能出口到GB(英格兰、苏格兰和威尔士)市场。从2023年7月1日开始,原来需要通过公告机构CE证书出口的医疗器械,要继续出口到GB市场,需要取得获认可的英国认证机构签发的UKCA的证书。
2)对于自我宣告类产品,在2021年1月1日开始就可以按照UK MDR 2002的要求来准备技术文件和相关支持性材料,以完成自我宣告,加贴UKCA标记。
UKCA标志技术文档的要求基本同欧盟CE标志的要求一样,最大的区别在于UK符合性声明(UK DOC)中需要注明对应的英国法规以及使用的英国标准。而现阶段,参考官方发布的指定标准designated standards清单可以看出,英国标准同欧盟标准基本保持一致。
同时,MHRA也更新了器械注册的规定。在脱欧之前,需要在MHRA注册的器械只包括I类器械,通用类的IVDD以及定制器械。但是脱欧后,MHRA要求所有类别的医疗器械都需要在MHRA进行注册。不过MHRA给出了为期一年的过渡期,基于产品风险等级高低,分别是4个月,8个月和12个月。
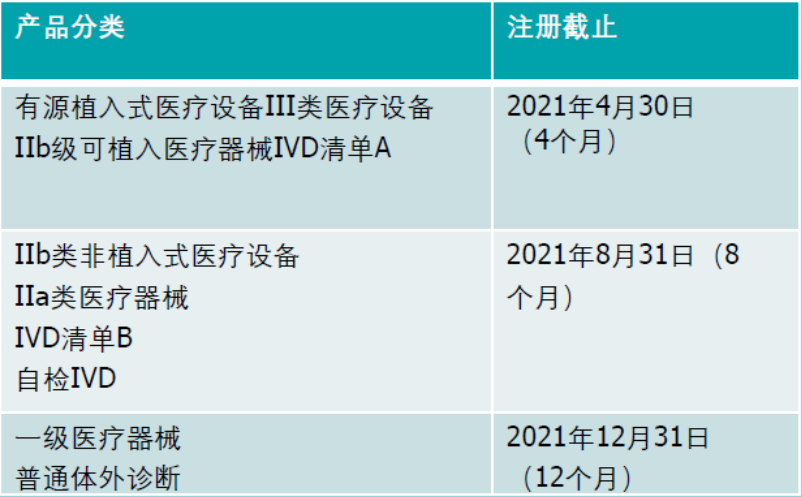
对于中国的医疗器械制造商,MHRA注册作为加贴UKCA标记确保产品持续合规的出口英国市场的关键一步,需要指定专业英国法规负责人来实施。
二、UKCA认证流程
1.确定适用的英国法规与标准
2.自我验证产品符合性
3.确定是否需要英国公告机构进行合格评定
4.检测产品的符合性
5.保存所需的技术文档
6.产品粘贴UKCA标志并签发UKCA DoC

三、UKCA适用规则
在大多数情况下,必须在产品本身或包装上使用UKCA标志。在某些情况下,它可能被放在手册或其他支持文档上。这将根据适用于产品的具体规定而有所不同。
一般适用规则:
a. UKCA标志只能由制造商或授权代表(在相关法例允许的情况下)放置在产品上;
b. 当贴上UKCA标志时,制造商或授权代表就需要对产品符合相关法律的要求负全部责任;
c. 只能使用UKCA标志来显示产品符合相关的英国法律;
d. 制造商或授权代表不能在产品上放置可能对第三方造成误解UKCA标志意思或形式的任何标记或标识;
e. 不得在产品上附加其他影响UKCA标志的可见性、易读性或含义的标记;
f.除非法律规定,否则不能在产品上使用UKCA标志。
四、UKCA标志的要求
1.UKCA标记中的字母必须与以下版本的比例成比例缩放
2.UKCA标记的最小高度为5mm-除非相关法律规定了不同的最小尺寸
3.UKCA标记须清晰可见(自2023年1月1日起,必须永久粘贴)
英国UKCA标志的正式实施,从中国出口欧盟需要CE认证的产品如果出口英国将需要进行UKCA认证,增加认证成本。
因此相关产品出口企业需要重点关注,及时获取贸易方对相关产品认证要求,提前准备认证材料,尽快完成产品认证,以防因此造成不必要的损失。
UKCA合规过程中,我们可以提供:
英国代理人
英国MHRA注册
UKCA的技术文件更新或者编撰
英国认证机构UKCA认证评审辅导
CE认证、欧盟授权代表
策划应对欧盟和英国市场准入最优方案
- 美国FDA
- 暂无标签




