根据商务部12号公告,自4月26日起,非医用口罩和部分医疗物资出口实施商务部白名单管理。
那么,口罩等防疫物资生产企业如何申请商务部白名单?
4月26日,商务部发布通知,防疫物资生产企业可以向本地商务局申请加入商务部白名单,并提交相关表格和证明材料。
通知

关于组织做好审核确认符合国外标准认证或注册的防疫物资生产企业名单有关工作的通知
各省、自治区、直辖市及新疆生产建设兵团商务主管部门:
为做好《商务部 海关总署 国家市场监督管理总局关于进一步加强防疫物资出口质量监管的公告》(2020年第12号)的落实工作,现就审核确认符合国外标准认证或注册的防疫物资生产企业名单有关工作通知如下:
请各地方商务主管部门组织本地防疫物资生产企业自愿填报有关表格并提交相关证明材料(非医用口罩生产企业填写附件1,医用口罩等5类医疗物资生产企业填写附件2)。
地方商务主管部门会同本地医疗物资商业出口工作机制有关成员单位初步审核后,以工作机制办公室名义(本地商务主管部门代章)将汇总表(含电子版)统一报送至国家医疗物资商业出口工作机制办公室(商务部外贸司),同时抄送中国医药保健品进出口商会。
原则上每周报送一次,截止时间为每周三17:00。
附件:
1.取得国外标准认证或注册的非医用口罩生产企业清单.xlsx
2.取得国外标准认证或注册的医疗物资生产企业清单.xlsx
国家医疗物资商业出口工作机制办公室
2020年4月26日
附件1:

填写说明:
1.填报范围仅限于获得国外认证或注册的非医用口罩;
2.请按产品填写,每个产品一行;
3.“企业名称”栏请务必填写中英文名称,同一家企业的多个产品请依次填写,企业名称列不合并单元格;
4.“产品名称”请列明中英文具体名称、规格、型号等;
5.请务必提交本表中已填写的国外认证关键材料扫描版,包括认证证书、检测报告等,并以证书名称命名该文件;
6.相关文件请统一放置到一个文件夹中,文件夹以企业中文名称命名,相关资质文件命名方式为:序号+企业中文名称缩写+产品名称+证书或检测报告名称。
附件2:
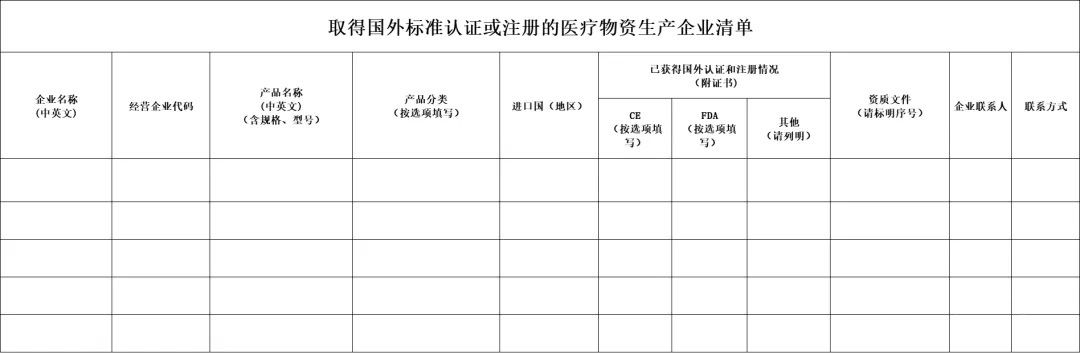
注:
1.仅限4月1日(含)以后签订合同且出口产品未取得我国医疗器械产品注册证书的企业填写;
2.请填报企业务必提供已填报的国外标准认证资料扫描件,及外方接受所购产品标准和质量的相关证明。
填写说明:
1.填报范围仅限于五大类医用物资,即新冠病毒检测试剂、呼吸机、医用防护服、医用口罩、红外体温计;
2.请按产品填写,每个产品一行;
3.“企业名称”栏请务必填写中英文名称,同一家企业的多个产品请依次填写,企业名称列不合并单元格;
4.“产品名称”请列明中英文具体名称、规格、型号等,并注明无菌或非无菌;
5.同一产品出口不同国家(地区),请在“进口国(地区)”单元格中合并填写,无须每个国家一行;
6.请务必提交本表中已填写的国外认证和注册文件,在“资质文件”列的同一个单元格中按序号列明;
7.本表格中已填写的“资质文件”,请统一放置到一个文件夹中,文件夹以企业中文名称命名,相关资质文件命名方式为:序号+企业中文名称缩写+产品名称+证书或检测报告名称,序号请务必与表格中“资质文件”列的序号相同。
8.其他:原则上产品出口应满足进口国标准,如未在进口国注册,请提供对方国授权进口许可的相关证明文件并在合同中约定。
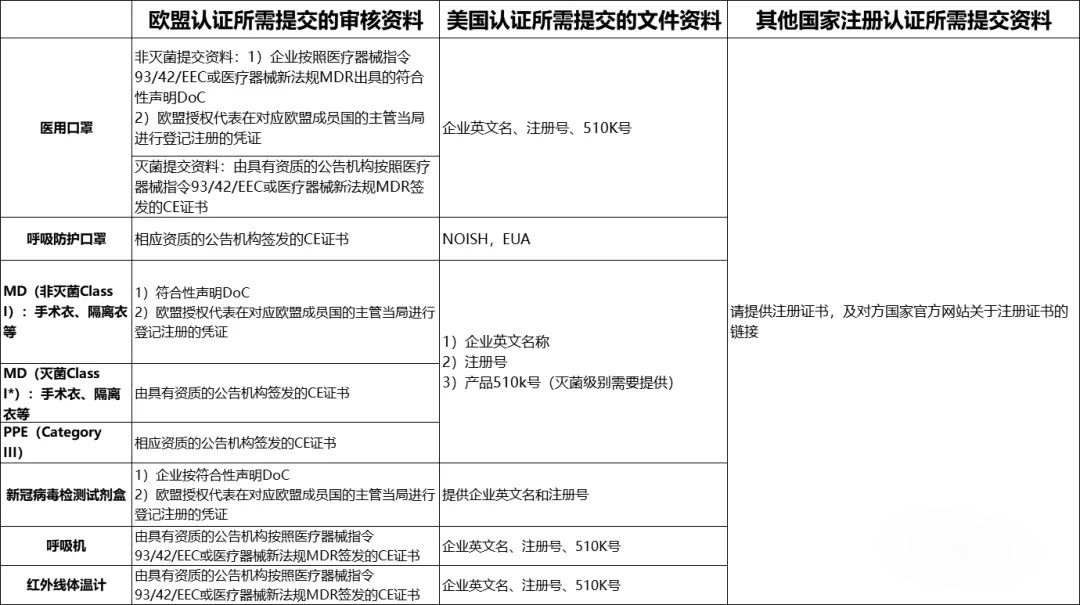
注明:主要应急物资认证及审核资料,请大家对照这个按照产品类别,提交完整资料,便于加快审核。建议一类产品一个文件夹,每个文件夹里面按照注册国别对提供的材料进行编号。
医用口罩 防护口罩,防护服,隔离衣,隔离面罩,隔离眼罩,新冠诊断试剂等。
我们提供服务: 欧盟CE认证、欧盟授权代表、欧盟主管当局注册、CE技术文件编写、美国FDA注册、FDA510k申报、EUA申请,美国Nelson检测、加拿大MDEL申报,国内注册证,生产许可证,GMP辅导,ISO9001/13845体系认证咨询等,欢迎垂询 张小姐 1366 1555 246。- 医疗器械
- 暂无标签




