为了确保产品可靠和用户安全,世界上主要经济体都制定了医疗器械市场准入的要求。
纵观所有的市场准入程序的设置框架,可以肯定的说产品检验检测在其中都至关重要。
按照欧盟MDR 2017/745/EU的规定,欧盟依据医疗器械的风险等级不同采取不同的合格评定路径来实现器械加贴CE标志,如图1所示。
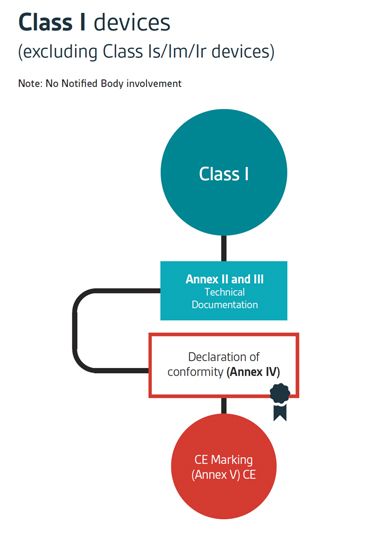
普通I类( 灭菌、非测量和非重复使用)医疗器械的合格评定模式就是基于技术文件来签发符合性声明,然后加贴CE标志。
可以看出技术文件非常关键,那么技术文件的结构通常包括哪些内容呢?
按照MDR法规的条文,技术文件通常包括如下几条:
1. 器械描述和规范,上一代或相似产品的参照
2. 制造商提供的信息(标签、说明书等)
3. 设计和制造信息
4. 基本安全和性能要求
5. 风险收益分析和风险管理
6. 产品验证和确认:临床前评价+临床评价
7. 上市后监督计划和报告
MDR法规和MDD相比较,尤其临床前评价方面,其要求与MDD时比较都有显著提高。 临床评价解决的是产品的设计和预期用途在临床使用时候能够实现,是否有风险产生,是否安全。而临床前评价则是要解决产品的设计开发和生产制造出来的产品是否满足欧盟标准和国际标准的相关要求,这包括安全方面,也包括产品性能方面。
临床前评价通常包括试验结果,如工程、实验室、模拟使用和动物试验:
- 器械生物相容性,包括与患者或使用者直接或间接接触的所有材料识别;
- 物理、化学和微生物表征;
- 电气安全和电磁兼容性;
- 软件验证和确认;
- 稳定性,包括产品有效期;
- 运输对产品的影响;
- 性能和安全性。
如果医疗器械产品没有对上述方面进行识别,并在必要时进行检测并将符合性证据纳入技术文件,那对于产品的性能和安全性的评价就失去最底层的证据。
医疗器械检测是产品认可上市前的必要环节,是保证医疗器械合格走向市场的最后一道关卡,其重要性可想而知。

FDASUNGO聚焦于检验检测服务的技术平台,经过了两年多的发展,目前已经建成了上海实验室、合肥实验室两个检测实验场地,可以为客户进行手术衣、隔离衣、医用手套、医用口罩等防疫物资性能检测,轮椅车、代步车、拐杖、助行器等康复医疗器械性能检测、包装验证和模拟运输等无菌医疗器械产品包装通用检测。目前支持的检测项目见下表:
|
序号 |
检测项目 |
|
1 |
手术衣/隔离衣(灭菌/非灭菌)美标PB70标准测试 |
| 2 |
手术洞巾(灭菌/非灭菌)美标PB70标准测试 |
|
3 |
医用口罩(灭菌/非灭菌)美标ASTMF 2100标准测试 |
| 4 |
医用手套(灭菌/非灭菌)美标ASTM标准测试 |
| 5 |
避孕套美标测试 |
| 6 |
医用口罩〔灭菌/非灭菌)欧标EN14683标准测试 |
|
7 |
医用手套(灭菌/非灭菌)欧标EN455标准测试 |
|
8 |
手术衣/隔离衣(灭菌/非灭菌)欧标EN13795标准测试 |
|
9 |
病毒采样拭子欧标测试 |
|
10 |
无菌医疗器械包装验证全套测试 |
|
11 |
无菌医疗器械运输验证全套测试 |
|
12 |
无菌医疗器械灭菌验证全套实施方案 |
|
13 |
电动轮椅ISO7176系列标准测试 |
|
14 |
手动轮椅ISO7176系列标准测试 |
|
15 |
电动轮椅EN12184标准测试 |
|
16 |
手动轮椅EN12183标准测试 |
|
17 |
助行器和拐杖等产品的欧标测试 |
|
18 |
鞋套/CPE鞋套/隔离鞋套性能测试 |
|
19 |
纱布叠片/无纺布套装性能测试 |
|
20 |
纱布卷/纱布球/脱脂纱布性能测试 |
|
21 |
弹性绷带性能测试 |
|
22 |
创可贴性能测试 |
|
23 |
SMMS检查裤/妇科短裙/短裤性能测试 |
|
24 |
无纺布片/无纺布套装性能测试 |
|
25 |
塑料袍/手术体位垫/铺单/PE膜PE袍/纸膜复合床单性能测试 |
|
26 |
无纺布与PE膜复合隔离衣性能测试 |
|
27 |
腹部垫/CPE隔离衣性能测试 |
|
28 |
垫单/产包性能测试 |
|
29 |
铺巾/工作服性能测试 |
|
30 |
隔离服性能测试 |
|
31 |
冷敷贴性能测试 |
|
32 |
防护面罩性能测试 |
|
33 |
抗病毒口罩性能测试 |
|
34 |
手术单性能测试 |
|
35 |
婴儿纸尿裤性能测试 |
|
36 |
女性纸尿裤性能测试 |
|
37 |
助步器产品性能测试 |
|
38 |
假肢性能测试 |
|
39 |
护具性能测试 |
|
40 |
洗澡椅、淋浴椅性能测试 |
|
41 |
造口袋性能测试 |
|
42 |
真空拔罐器性能测试 |
|
43 |
可重复使用冷热敷理疗袋性能测试 |
|
44 |
上肢支具性能测试 |
|
45 |
石膏衬垫性能测试 |
|
46 |
矫形器性能测试 |
|
47 |
夹板性能测试 |
|
48 |
护颈仪性能测试 |
|
49 |
康复训练牵引器性能测试 |
|
50 |
空气压力波气囊性能测试 |
|
51 |
三球肺活量训练器性能测试 |
|
52 |
冲洗袋性能测试 |
|
53 |
气态减重步态训练系统性能测试 |
|
54 |
浴室扶手性能测试 |
|
55 |
马桶椅配件性能测试 |
|
56 |
护脐带性能测试 |
|
57 |
护手腕/肘部支具性能测试 |
|
58 |
EO残留测试性能测试 |
|
59 |
洁净车间测试性能测试 |
|
60 |
产品无菌测试性能测试 |
综上,FDASUNGO认为不论是从法规本身的要求出发,还是从降低制造商自身风险出发,开展医疗器械测试,将检测报告纳入技术文件都是必须的,也是以最小的投入来控制自身风险的最佳方式。
FDASUNGO可供:欧盟/美国标准检测、 CE认证、欧盟授权代表、欧盟注册、CE技术文件编写/编制符合MEDDEV 2.7.1 Rev 4要求的英文临床评估报告、欧盟自由销售明、FDA注册、FDA510K申报、英国UKCA、瑞士代表/注册、ISO9001/13485认证咨询、国内产品注册证/生产许可证、MDSAP验厂辅导等。认证检测咨询一站式服务,合作垂询 1366-1555-246。
- 美国FDA
- 暂无标签

