常常感慨这场COVID-19感觉如同二战时风卷残:意大利沦陷,西班牙沦陷,当然还有米国沦陷。。。。。
三十年河东,三十年河西,在这场“三战”中,口罩成为硬通货,一时间光芒万丈,豪气干云,FDASUNGO所在的城市有一个口罩厂年前还在苦哈哈的准备破产清算,突然新冠病毒骤然而至,价格从2毛涨到4块。
经过全国人民的奋力抗战,特别是很多医务人员逆行而上,壮怀激烈,为我们铸起了一道道病毒防火墙。
疫情基本控制后,我们也开始反哺那些救助过我们的国家和人群,积极把生命、血泪浸渍的经验和产品向外推广,于是您懂的,各种李鬼纷至沓来,假证做的比真的还象真的。
FDASUNGO经常参与一些合规的内容审核,在看到各种各色的证书中,不避浅陋,简单说说如何辨别口罩的CE证书:
1.什么是CE
CE是法语的缩写,英文意思为“European Conformity即欧洲共同体。在欧盟市场“CE”标志属强制性认证标志,不论是欧盟内部企业生产的产品,还是其他国家生产的产品,要想在欧盟市场上自由流通,就必须加贴“CE”标志,以表明产品符合欧盟《技术协调与标准化新方法》指令的基本要求。这是欧盟法律对产品提出的一种强制性要求。
请记住,CE是对着很多不同的指令或法规,您看到口罩上有CE标志,并不一定符合MDR 2017/745法规。
2.口罩应符合什么CE要求
工欲善其事,必先利其器。我们先简单看看国内口罩分类方式:

其实欧洲也是分民用和医用的口罩,只是人家不象我们分的这么细,全部并到一个标准里去了。
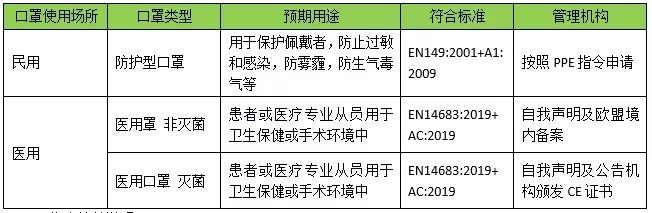
2.1 PPE指令简单说明
按照2016/425 PPE指令ANNEX I:RISK CATEGORIES OF PPE,防护口罩属于III级
根据2016/425 PPE指令Article 19: Conformity assessment procedures
而新指令和作废的89/686/EEC PPE指令在认证方式上出现了差异,老的89/686/EEC PPE指令可以直接采用EU Type-examination也即型式试验,而新的指令明确要求除了这一个不充分,还需要加模块C2或模块D。
另外新的PPE指令针对防护口罩的证书必须是由公告机构颁发,在PPE证书上必须看到公告机构的代码。
在2016/425 PPE指令Article 47中针对新旧指令转换期间出了一个过渡要求:
也就是说2019年4月21日前出的EU Type-examination还可以认为是有效的,有效期至2023年4月21日前。
2.2医疗器械指令或法规的说明
目前欧盟医疗器械法规处于变化期,2017年5月5日欧盟正式发布了新版医疗器械法规–EU 2017/745(MDR),这个法规将取代欧盟现行的医疗器械指令93/42/EEC以及有源植入性医疗器械指令90/385/EEC,新的MDR法规也在2020年5月26日正式强制实施。
注意:MDR是法规,不是指令。
所以当前I类非灭菌医用口罩仍然可以用MDD指令去备案,但自2020年5月26日起要满足MDR法规,所以FDASUNGO建议当前I类非灭菌医用口罩备案时直接符合MDR法规。
在I类非灭菌医用口罩申请CE时也是最容易出现很多问题:
(1)用第三方对CE技术文档的检查报告作为CE证书
(2)用欧盟代表的声明作为CE证书
(3)甚至用检测报告作为CE证书
再次付责任的声明:I类非灭菌产品是没有CE证书的,都由制造商进行自我宣称CE符合性,但这个并不意味着制造商只要出一个声明就OK了,可以直接出口欧盟了。No,企业必须准备一套CE技术文档,还得是英文版存于欧盟代表处以备主管当局核查,同时进行欧代所在药监局进行产品注册。
FDASUNGO曾听到某某客户跟我说,我们当时CE技术文件只要中文版,英文版根本没有、不需要,当即刷新了我的认知,原来我是如此out…..
3.医疗器械符合性声明DoC的介绍
医疗器械符合性声明应至少包括以下内容:
3.1制造商和授权代表的名称、地址、注册商标名
3.2声明EU符合性声明由制造商全权负责签发
3.3产品名称及产品代码以及器械的预期用途。
3.4产品的风险等级
3.5声明DoC所涵盖的器械符合MDR法规
3.6公告机构的名称及代号、对所执行符合性评估程序的描述以及公告机构签发的对应证书的识别信息。
3.7 DoC的签发地点和签发日期、签署人的姓名和职位。
4.如何查询公告机构的资质
您可以通过以链接去查公告机构的资质授权:
通过首字母或公告代号去查询,这下子李鬼李逵傻傻分得清楚了:
比如我们用最近比较流行的某意大利证书去查:
Oh, my God,你还看到他们家发的PPE指令证书呢,一查原来没有资质。再一看,噢,原来人家写了这样一句话:
确实写得很清晰,制造商负责与公告机构沟通通过CE符合性评价程序获得正式的的CE证书。
5.医用口罩符合的欧盟标准
入乡随俗,我们的产品进入欧盟市场自然也得人家的游戏规则,同样,医用口罩也是这样的道理:
产品标准:
EN14683:2019+AC:2019 Medical Face Masks–Requirements and test methods
生物相容性标准:
EN ISO 10993-1:2009Biological evaluation of medical devices — Part 1: Evaluation and testing within a risk management process
EN ISO 10993-5:2010 Biological evaluation of medical devices —Part 5: Tests for in vitro cytotoxicity
EN ISO 10993-10:2010 Biological evaluation of medical devices Part 10: Tests for irritation and skin sensitization
标签和说明书
EN ISO 15223-1:2016 Medical devices–symbols to be used with medical device labels, labelling and information to be supplied--- part 1: General requirements
EN 1041:2008+A1:2013 Information supplied by the manufacturer of medical devices
6. EN 14683的简单介绍
EN 14683将口罩分成两个大的类别:Type I and Type II/IIR
I型医用器皿仅适用于患者和其他从使用来降低感染传播的风险,尤其是在传染病或流行病的情况中。
II型口罩主要供医疗专业从员在手术室或其他具有类似要求的医疗环境中使用。
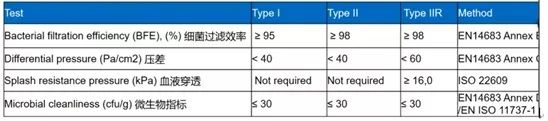
平时美国分类为二类的产品(例如外科手术口罩)需要先申请FDA510K,申请周期至少6-8个月
疫情期间口罩美国FDA注册
COVID-19应急口罩FDA代码,申请流程如下:(不适用N95口罩)
1)提供产品信息,进行产品类别判定并确定申请路径;
2)填写FDA申请表;
3)签署合约并支付代理费用,同时美国代理人服务签署和生效;
4)支付美金到美国FDA;
5)代理公司提交注册申请资料给美国FDA审批(企业注册和产品列名) ;
6)注册审批完成,获得批准号码;
7)代理公司颁发注册证明书;
8)项目结束(医疗器械FDA每自然年年底续费更新下一年度注册)。
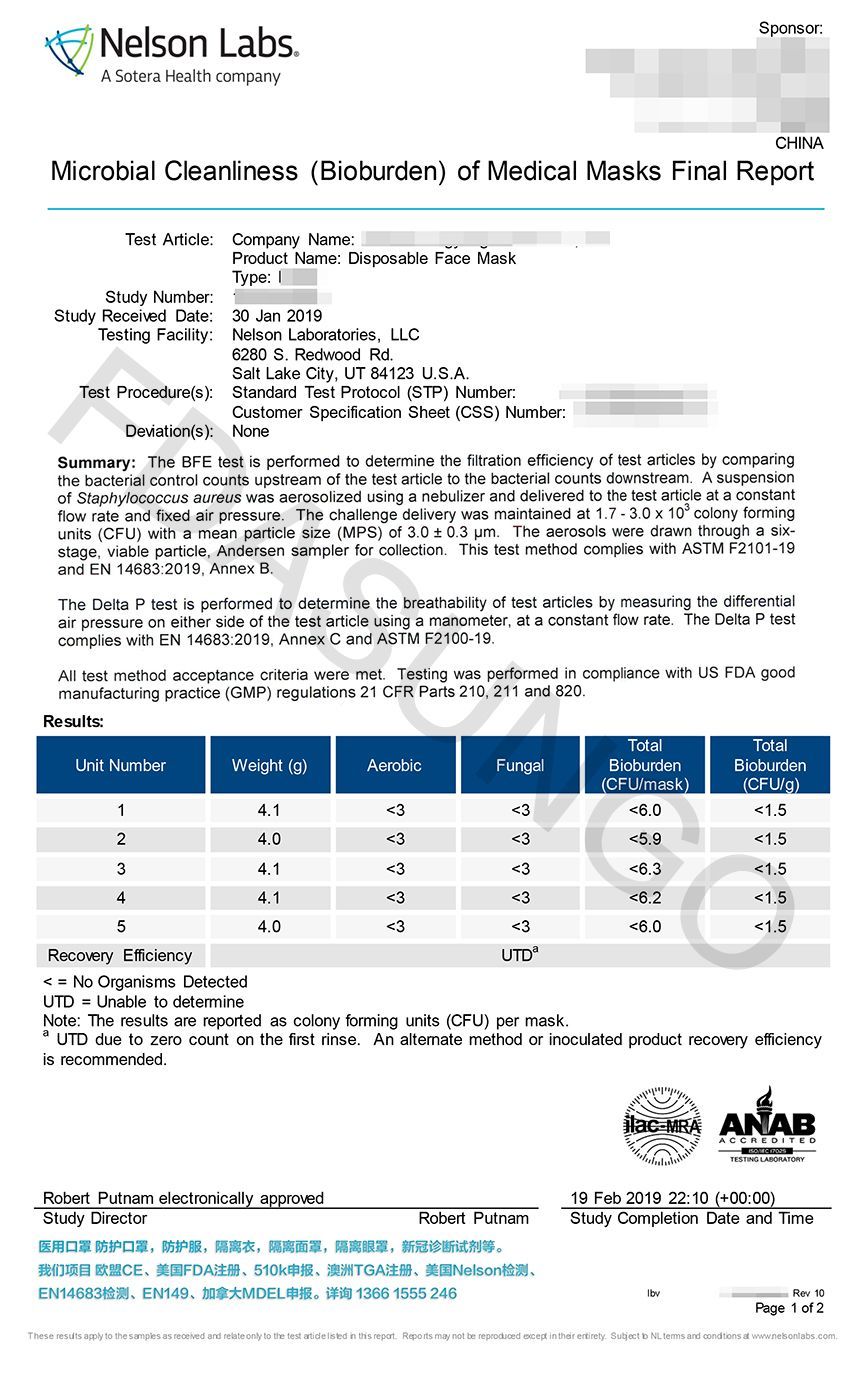
- FDA注册
- 暂无标签





